

映恩生物靶向HER2 ADC药物获批临床

11月21日,CDE官网显示,映恩生物研发的ADC产品DB-1303(BNT323)获批临床,拟用于治疗晚期/转移性实体瘤。此次获批为适应症拓展,是DB-1303在国内获批的第六个批件。此前今年1月,美国FDA授予DB-1303快速通道资格,用于治疗HER2过度表达的晚期、复发或转移性子宫内膜癌患者。
DB-1303是今年4月,映恩生物16.7亿美元授权给BioNtech的两款ADC之一,是由映恩生物专有的DITAC平台构建的第三代HER2 ADC药物。基于映恩生物DITAC技术平台构建,这种设计让ADC的血浆稳定性更好,在肿瘤组织特异性的释放毒素,并通过旁观者效应杀伤HER2阴性的癌细胞,最终达到有效性与安全性的更好平衡。实验室研究显示,DB-1303对于HER2阳性以及HER2低表达的肿瘤均有良好的抗肿瘤活性。
8月30日,映恩生物在Clinicaltrials.gov网站上注册了DB-1303的三期临床试验(DYNASTY-Breast02),用于治疗转移性乳腺癌。
DB-1303在早期临床中表现出很好的治疗潜力,对于HER2低表达乳腺癌的ORR为38.5%(5/13),DCR为84.6%(11/13)。
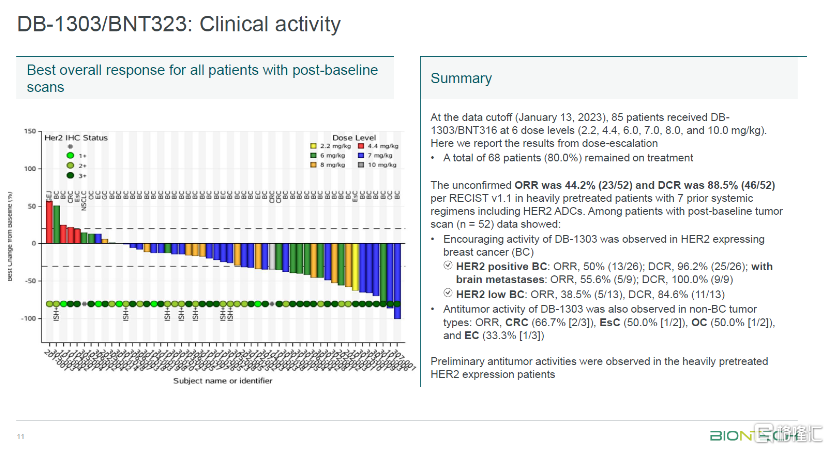
2023年11月7日BioNtech研发日活动上,在今年引进的4款ADC药物中,DB-1303有望成为潜在的最佳疗法。DB-1303在HER2 高低表达的乳腺癌中均显示出可比性的响应率,此数据也用以支持正在开展三期临床开发;在子宫内膜癌的中差异性临床开发,也取得不错的响应率,有望加速其获得上市批准。
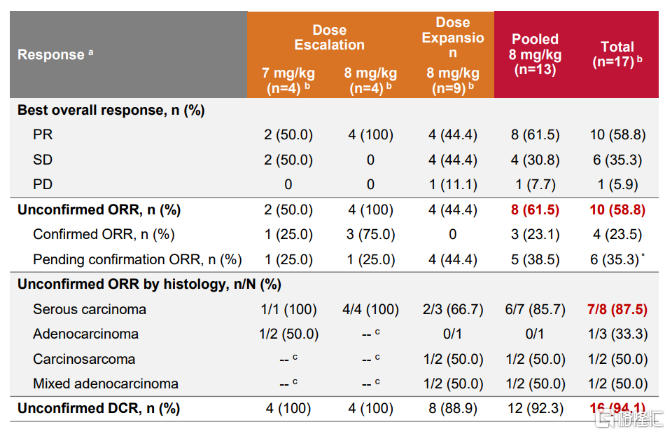
2023 ESGO年会上,映恩生物公布DB-1303正在进行的1/2a期临床(DB-1303-O-1001研究)的最新数据。数据显示:截至2023年05月08日,DB-1303在既往多线经治的HER2表达(IHC 3+或IHC 2+或IHC 1+或ISH+)的复发或转移性EC受试者中表现出良好的抗肿瘤活性,客观缓解率(ORR)达到58.8%,疾病控制率(DCR)达到94.1%;安全性方面未观察到导致永久停药的TEAE,未观察到与研究药物相关的SAE,最常见的TEAE包括恶心、呕吐和疲乏。
映恩生物深耕ADC药物的创新研发,开发了包含DITAC, DIMAC和DISAC在内的多个具有独立知识产权的ADC技术平台,其中DITAC(Duality Immune Toxin Antibody Conjugate)技术平台,相比于目前国际领先的ADC技术平台,具有肿瘤靶向性药物释放更精准、疗效更好、安全性更高以及治疗窗口更宽等显著优势。目前基于DITAC平台,已开发了近10款前沿治疗ADC药物分子。
研发管线(部分)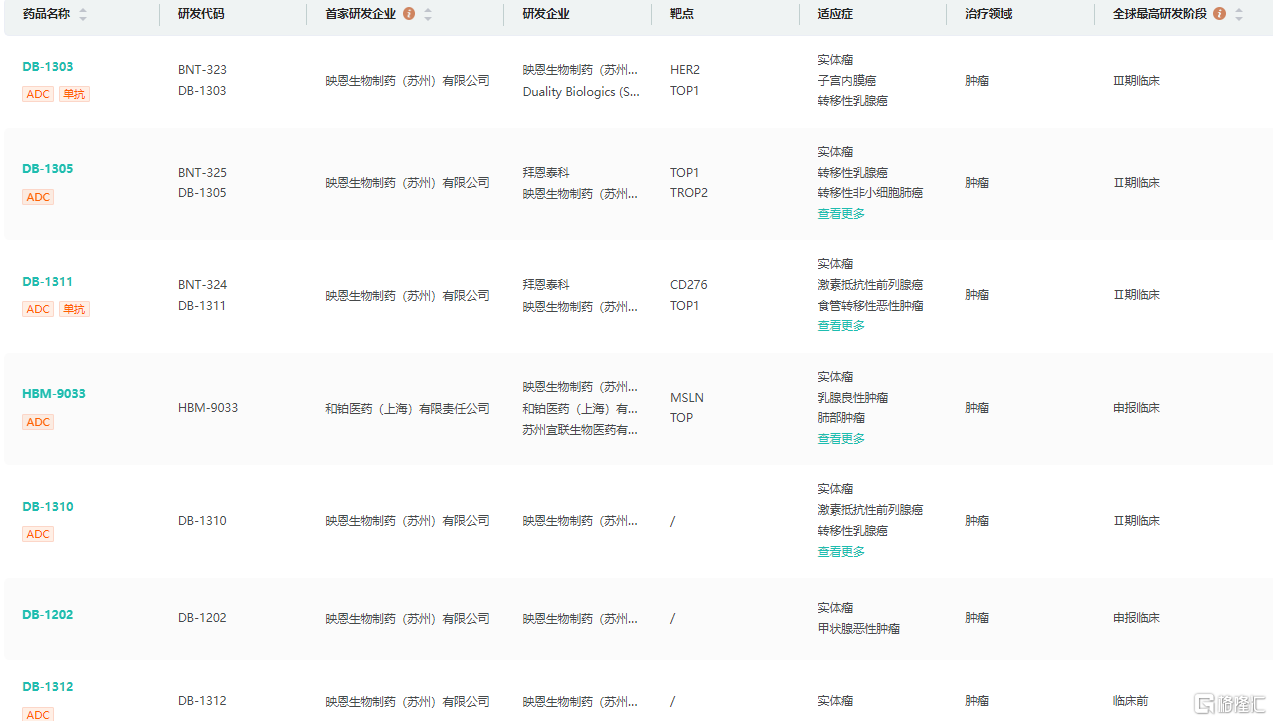 截图来源:药融云全球药物研发数据库
截图来源:药融云全球药物研发数据库
格隆汇声明:文中观点均来自原作者,不代表格隆汇观点及立场。特别提醒,投资决策需建立在独立思考之上,本文内容仅供参考,不作为实际操作建议,交易风险自担。


