

FDA批准武田Adzynma酶替代疗法用于治疗先天性血栓性血小板减少性紫癜(cTTP)
11月9日,武田公司宣布美国美国食品药品监督管理局(FDA)已经批准Adzynma(ADAMTS13,重组-krhn)用于成人和儿童先天性血栓性血小板减少性紫癜(cTTP)患者的预防性和按需治疗。
Adzynma是第一个也是唯一一个FDA批准的重组ADAMTS13 (rADAMTS13)蛋白,旨在通过替换有缺陷的ADAMTS13酶来解决cTTP患者未满足的医疗需求。
cTTP是一种极其罕见的慢性凝血障碍,由ADAMTS13酶缺乏引起。3它与急性事件和使人虚弱的慢性症状或血栓性血小板减少性紫癜(TTP)表现有关,包括血小板减少症、微血管病性溶血性贫血、头痛和腹痛。3,4,5如果不进行治疗,急性TTP事件的死亡率超过90%。
武田公司新闻资讯查询

图片来源:药融云新闻资讯数据库
俄亥俄州立大学Wexner医学中心内科教授、美国血栓性微血管病联盟(USTMA)联合主任兼Adzynma临床试验研究员Spero R. Cataland医学博士说:“近几十年来,在更好地了解ADAMTS13缺乏和cTTP之间的联系方面取得了重大进展,最终导致我们终于有了一个FDA批准的治疗这种罕见疾病患者的治疗方案。”
Adzynma为患者提供了一种替代其有缺陷的ADAMTS13酶的治疗选择,并提供了有利的疗效和安全性,与当前基于血浆的治疗相比,减少了给药时间和剂量。今天标志着一项重大成就,为cTTP患者群体提供了新的可能性。
FDA对Adzynma的批准得到了cTTP第一次随机、对照、开放、交叉3期试验的疗效、药代动力学、安全性和耐受性数据分析以及延续试验数据所提供的全部证据的支持。在3期试验中,患者每隔一周或每周接受40 IU/kg Adzynma IV或基于血浆的治疗,基于在第1-6个月(第1期)登记时的方案,过渡到第7-12个月(第2期)的替代治疗,并且所有患者在第13-18个月(第3期)接受Adzynma。
在接受Adzynma预防性治疗时,没有患者出现急性TTP事件(n=37),而在接受基于血浆的治疗的患者中,有1例出现急性TTP事件(n=38)。1在3期研究对照的第1期和第2期,接受Adzynma治疗的患者中未报告亚急性TTP事件,相比之下,接受基于血浆的治疗的4名患者中有5例亚急性TTP事件。在延续期(第3期),两名接受Adzynma预防治疗的患者发生了两起亚急性事件。
接受Adzynma治疗的患者血小板减少症表现的平均年化事件率(SD)为2.0(4.706)(9/37患者出现表现),而接受基于血浆的治疗的患者为4.44(6.312)(19/38患者出现表现)。1虽然这种比较的临床意义尚不清楚,但血小板减少症是TTP的一种表现,因此是疾病活动的一种重要生物标志物。
ADAMTS13全球同靶点适应症分析
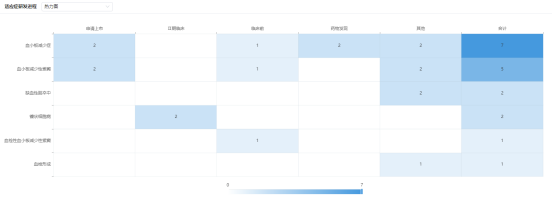
图片来源:药融云靶点格局数据库
Adzynma是ADAMTS13蛋白的重组形式。在药代动力学评估中,与基于血浆的治疗相比,接受40 IU/kg Adzynma IV的患者(n=23)在单次输注后ADAMTS13活性增加了4至5倍。
与基于血浆的疗法相比,Adzynma显示出良好的安全性。最常见的不良反应(发生率> 5%)为头痛、腹泻、偏头痛、腹痛、恶心、上呼吸道感染、头晕和呕吐。接受Adzynma治疗的患者没有出现中和抗体。
关于Adzynma
Adzynma (ADAMTS13,recombinant-krhn)是一种人类重组“具有血小板反应蛋白基序13的去整合素和金属蛋白酶”ADAMTS13 (rADAMTS13),适用于成人和儿童先天性血栓性血小板减少性紫癜(cTTP)患者的预防性或按需酶替代治疗(ERT)。
药融云数据库显示,Adzynma之前曾被美国FDA授予孤儿药物指定(ODD ),用于治疗和预防TTP,包括其获得性特发性和继发性形式,以及快速通道和罕见儿科疾病指定。美国FDA授予武田罕见儿科疾病凭证,用于Adzynma的批准。Adzynma还被欧洲药品管理局(EMA)和日本厚生劳动省(MHLW)授予ODD,用于治疗TTP。
格隆汇声明:文中观点均来自原作者,不代表格隆汇观点及立场。特别提醒,投资决策需建立在独立思考之上,本文内容仅供参考,不作为实际操作建议,交易风险自担。


